如图所示是800℃时,X、Y、Z三种气体的浓度(c)随时间(t)的变化情况,t2是反应达到平衡的时间,写出反应的化学方程式:______.
题型:不详难度:来源:

答案
当反应进行到2min时,△n(X)=0.4mol,△n(Y)=0.2mol,△n(Z)=0.6mol,
则△n(X):△n(Y):△n(Z)=2:1:3,参加反应的物质的物质的量之比等于化学计量数之比,
则反应的方程式为:2X
 Y+3Z,故答案为:2X
Y+3Z,故答案为:2X Y+3Z.
Y+3Z.举一反三

| A.p3>p4,y轴表示A的转化率 |
| B.p3<p4,y轴表示混合气体的密度 |
| C.p3<p4,y轴表示B的质量分数 |
| D.p3<p4,y轴表示混合气体的平均摩尔质量 |
| 在某个容积为2.0L的密闭容器中,在T℃时按下图1所示发生反应: mA(g)+nB(g)  pD(g)+qE(s),△H<0(m、n、p、q为最简整数比). pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).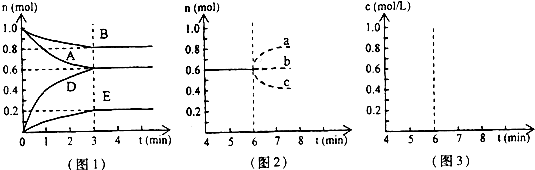 (1)图1所示,反应开始至达到平衡时,用D表示的平均反应速率为______. (2)T℃时该反应的化学平衡常数K的数值为______. (3)反应达到平衡后,第6min时: ①若升高温度,D的物质的量变化曲线最可能的是______(用图2中的a~c的编号作答); ②若在6min时仍为原平衡,此时将容器的容积压缩为原来的一半.请在图3中画出6min后B浓度的变化曲线______. 4)在T℃时,相同容器中,若开始时加入0.4molA、0.8molB、0.9molD和0.5molE0.5mol,反应达到平衡后,A的浓度范围为______. (5)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的是______. A.化学反应速率理论可指导怎样在一定时间内快出产品 B.有效碰撞理论可指导怎样提高原料的转化率 C.勒夏特列原理可指导怎样使用有限原料多出产品 D.催化剂的使用是提高产品产率的有效方法 E.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益. |
工业上合成尿素是用CO2和NH3在一定条件下合成,其反应方程式为2NH3+CO2
|
 CO(NH2)2+H2O,当氨碳比
CO(NH2)2+H2O,当氨碳比 ,CO2的转化率随时间的变化关系如图所示,下列说法错误的是( )
,CO2的转化率随时间的变化关系如图所示,下列说法错误的是( )

