工业生产纯碱
工业生产纯碱
纯碱(学名碳酸钠)实际上是盐,由于它在水中发生水解作用而使溶液呈碱性。纯碱易溶于水,呈强碱性,能提供Na+离子。这些性质使它们被广泛地用于制玻璃、肥皂、纺织、印染、漂白、造纸、精制石油、冶金及其他化学工业等各部门中。
碳酸钠在自然界中存在相当广泛。一些生长在盐碱地和海岸附近的植物中含有碳酸钠,可以从植物的灰烬中提取;当冬季来临时,碱湖中所含的碳酸钠结晶析出,经过简单的加工就可以使用。
世界上最早是通过路布兰法实现了碳酸钠的工业生产。其生产原理是:
用硫酸将食盐转变成硫酸钠
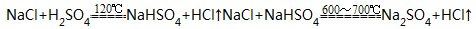
将硫酸钠与木炭、石灰石一起加热,反应生成碳酸钠和硫化钙

存在原料利用不充分、成本较高、设备腐蚀严重等
过碳酸钠俗称固体双氧水,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,它的制备原理和路线如下:2Na2CO3 + 3H2O2 =2Na2CO3·3H2O2 △H<0 
回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是_________________。
(2)下列物质可使过碳酸钠较快失效的是_________________。
a.MnO2 b.H2S c.稀硫酸 d.NaHCO3
(3)加入NaCl的实验操作名称是_________________;作用是_________________。
(4)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与Fe3+生成稳定的配合物,Fe3+对反应的不良影响是_________________。
(5)反应的最佳温度控制在15℃~20℃,温度偏高时造成产率低可能是_________________,温度偏低时造成产率低的可能是_________________。
(6)以上流程中遗漏了一步,造成所得产品纯度偏低,该步操作的名称是_________________。进行该操作的方法是:_________________。
(7)抽滤也称吸滤或减压过滤,是一种实验室常用的过滤方法(如图所示)。抽滤为什么能加快过滤,原因_________________。
纯碱(Na2CO3)在工业生产和生活中有重要应用,其实验室制法和工业制法如下:
【实验室制备纯碱】
①将饱和NaCl溶液倒入烧杯中加热,控制温度为30-35℃
②搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟
③静置、过滤得NaHCO3晶体
④用少量蒸馏水洗涤、抽干
⑤将所得固体转入蒸发皿中灼烧得Na2CO3固体
问题:
(1)反应将温度需控制在30-35℃,通常采取的加热方法为_________________ ;控制该温度的原因是
__________________;
(2)静置后只析出NaHCO3晶体的原因是____________________。
【工业制备纯碱】
(3)沉淀池中反应的离子方程式为_________________________;
(4)循环(I)、 循环(Ⅱ)中物质的化学式分别为_____________________。两种制备纯碱的方法中,共同涉及的化学反应方程式为_________________________。工业生产纯碱的工艺流程示意图如下 
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A_________B_________
(2)实验室提纯粗盐的实验操作依次为:取样、_________、沉淀、_________、_________、冷却结晶、_________、烘干。
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是__________________。碳酸化时没有析出碳酸钠晶体,其原因是__________________。
(4)碳酸化后过滤,滤液D最主要的成分是_________(填写化学式),检验这一成分的阴离子的具体方法是:__________________。
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨。加石灰水后所发生的反应的离子方程式为:__________________滤液D加石灰水前先要加热,原因是__________________。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:__________________(注明你的表达式中所用的有关符号的含义)工业生产纯碱的工艺流程示意图如下 
完成下列填空
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A_____________B____________
(2)实验室提纯粗盐的实验操作依次为:取样、________、沉淀、_________、__________、冷却结晶、_________、烘干。
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是____________。碳酸化时没有析出碳酸钠晶体,其原因是____________。
(4)碳酸化后过滤,滤液D最主要的成分是____________(填写化学式),检验这一成分的阴离子的具体方法是:______________________________。
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨。加石灰水后所发生的反应的离子方程式为:_____________________滤液D加石灰水前先要加热,原因是________________________。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:__________________(注明你的表达式中所用的有关符号的含义)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制 碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式:_______________________________________________________;
(2)写出“联合制碱法”有关反应的化学方程式:____________________________________________;
(3) CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?__________________________________________________________;
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:
原子利用率(%) =________________________________。碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+ 、Cl-和SO42-等杂质,提纯工艺路线如下: 
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示: 
回答下列问题:
(1)滤渣的主要成分为____。
(2)“趁热过滤”的原因是____。
(3)若在实验室进行“趁热过滤”,可采取的措施是____(写出1种)。
(4)若“母液”循环使用,可能出现的问题及其原因是____。
(5)已知:
Na2CO3·l0H2O(s)=Na2CO3(s) +10H2O(g) △H1= +532. 36kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s) +9H2O(g) △H2= +473.63kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式__________________________________。工业制纯碱时,第一步通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠结晶。它的反应原理可以用下面的方程式表示:
NH3+CO2+H2O==NH4HCO3,NH4HCO3+NaCl(饱和)==NaHCO3↓+NH4Cl
以上反应的总结果是放热反应。下面设计了一个实验,用最简单的实验装置模拟实验这一过程,获得碳酸钠结晶。可供选择的实验用品有:稀盐酸、稀硫酸、浓氨水、氢氧化钠、消石灰、石灰石、氯化铵、食盐、蒸馏水和冰,以及中学化学实验常用仪器。实验装置示意图(包括反应时容器中的物质)如下,图中玻璃容器旁自左至右分别用A、B、C······符号标明(请见题后说明)
(1)请写出在图上A、B、C······各玻璃容器中盛放物质的化学式或名称。 A:__________________,B:___________________,C:__________________, D:__________________,E_____________________。
(2)利用在本题所提供的实验用品,如何判断得到的产品是碳酸氢钠的结晶,而不是碳酸氢铵或食盐结晶?_______________________________我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下: 
(1)上述生产纯碱的方法称_________ ,副产品的一种用途为____________ 。
(2)沉淀池中发生的化学反应方程式是_________________ 。
(3)写出上述流程中X物质的分子式________________________ 。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了____________(填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作是_________________ 。
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加____________ 。
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有_____________ 。
(a) 增大NH4+的浓度,使NH4Cl更多地析出 (b) 使NaHCO3更多地析出 (c) 使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度坐落在山东沿海地区的潍坊纯碱厂是我国重点大型企业,其生产工艺沿用我国化学侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下: 
①上述生产纯碱的方法称___________ ,副产品的一种用途为______________ 。
②沉淀池中发生的化学反应方程式是________________ 。
③写出上述流程中X物质的分子式___________________ 。
④使原料氯化钠的利用率从70%提高到90%以上,主要是设计了_____ (填上述流程中的编号)的循环。
⑤向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有___________ 。
A.增大NH4+的浓度,使NH4Cl更多地析
B.使NaHCO3更多地析出
C.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式:_______________
(2)写出“联合制碱法”有关反应的化学方程式:_____________________
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?_________________________
(4)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:原子利用率(%)=_________________工业生产纯碱的工艺流程示意图如下: 
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。 A_______,B_________。
(2)实验室提纯粗盐的实验操作依次为:取样、____ 、沉淀、____、____、冷却结晶、____ 、烘干。
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是_____________。碳酸化时没有析出碳酸钠晶体,其原因是______________。
(4)碳酸化后过滤,滤液D最主要的成分是____(填写化学式),检验这一成分的阴离子的具体方法是:_____________________。
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨。加石灰水后所发生的反应的离子方程式为:______________________, 滤液D加石灰水前先要加热,原因是______________________。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:_________ (注明你的表达式中所用的有关符号的含义)。在动物饲料中添加三聚氰胺,将提高饲料中的氮含量,让人误以为该饲料的蛋白质比较丰富,其营养价值实际上却没有增加关于三聚氰胺的合成,目前较多采用尿素法,因为此法成本低。尿素以氨气为载体,硅胶为催化剂,在380-400℃温度下沸腾反应,先分解生成氰酸(HCNO),并进一步缩合生成三聚氰胺生成的三聚氰胺气体经冷却捕集后得粗品,然后经溶解,除去杂质,重结晶得成品。下图是简单流程图,已知a、b为气体,且a极易溶于水,回答下列问题: 
(1)反应①的化学方程式为_____________________;
(2)物质b为_____________________,反应②的化学方程式为____________________________;
(3)相同状态下,产生的气体a和b的体积之比为________________________________;
(4)我国著名化学家候德榜先生发明的“侯氏制碱法”,因原料利用率高,并能进行连续生产,从而享誉中外。本实验具体操作过程中,应先通________________气体,再通_____________________气体;某同学进行了侯氏制碱的模拟实验,实验所用的饱和NaCl溶液中含溶质58.5 g,实验最后得到无水碳酸钠26.0g,则其产率为____________;该同学针对其实验结果,认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是___________________________________。工业生产纯碱的工艺流程示意图如下: 
完成下列填空:
(1)沉淀剂A来源于石灰窑厂,写出A、B的化学式。A__________________,B___________________。
(2)实验室提纯粗盐的实验操作依次为:取样、_______、沉淀、______、_______。
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象_______________。碳酸化时没有析出碳酸钠晶体,其原因是__________________。
(4)碳酸化后过滤,滤液D最主要的成分是_________________(填写化学式),检验这一成分的阴离子的具体方法:____________________________。
(5)向滤液D中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有__________________(填a、b、c字母) 。这样做使原料氯化钠的利用率从70%提高到90%以上,主要是设计了___________的循环,这就是有名的侯氏制碱法。
a.增大NH4+的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:_______________________(注明你的表达式中所用的有关符号的含义)。以食盐为原料进行生产并综合利用的某些过程如下图所示。 
(1)除去粗盐中的Ca2+、Mg2+和SO42-,加入下列沉淀剂的顺序是(填序号)________。
a.Na2CO3 b.NaOH c.BaCl2
(2)将滤液的pH调至酸性除去的离子是____________。
(3)电解饱和食盐水的离子方程式是_________________。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式
是_________
(5)纯碱在生产生活中有广泛的应用。
①纯碱可用于除灶台油污。其原因是(结合离子方程式表述)_________________。
②常温下,向某pH=11的Na2CO3溶液中加入过量石灰乳,过滤后所得溶液pH= 13。则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是_______________。
③工业上,可以用纯碱代替烧碱生产某些化工产品:如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是___________________(已知碳酸的酸性强于次氯酸)。碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(钝度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺路线如下 
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示 
回答下列问题
(1)滤渣的主要成分为_____________
(2)“趁热过滤”的原因是___________。
(3)若在实验室进行“趁热过滤”,可采取的措施是___________(写出一种)
(4)若“母液”循环使用,可能出现的问题及其原因是______________________。
(5)已知:
Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式______________________。以食盐为原料进行生产并综合利用的某些过程如下图所示。 
(1)除去粗盐中的Ca2+、Mg2+和SO42-,加入下列沉淀剂的顺序是(填序号)________。
a.Na2CO3 b.NaOH c.BaCl2
(2)将滤液的pH调至酸性除去的离子是___________。
(3)电解饱和食盐水反应的离子方程式是________________。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是____________。
(5)纯碱在生产生活中有广泛的应用。
①纯碱可用于除灶台油污。其原因是(结合离子方程式表述)_______________。
②常温下,向某pH= 11的Na2CO3溶液中加入过量石灰乳,过滤后所得溶液pH=13。则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是__________
③工业上,可以用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是___________________。(已知碳酸的酸性强于次氯酸)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式:______________;
(2)写出“联合制碱法”有关反应的化学方程式______________。
(3)CO2是制碱工业的重要原料,“联合制碱法”中CO2的来源于______________,“氨碱法”中CO2来源于______________。技术的发展与创新永无止境。我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如图所示 
(1)向沉淀池中要通入CO2和氨气,应先通入________(填化学式),原因是_________________
(2)沉淀池中发生反应的化学方程式是____________________
(3)母液中的溶质主要是________,向母液中通氨气,加入细小食盐颗粒,冷却析出副产品。通氨气的作用是____________________。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了____________(填上述流程中的编号)的循环;物质X是__________,从沉淀池中提取沉淀的操作是_______________
(5)写出煅烧炉中发生反应的化学方程式:____________________。
(6)这样制得的产品碳酸钠中可能含有的杂质是__________(填化学式),为检验该杂质的存在,具体操作是________________。以食盐为原料进行生产并综合利用的某些过程如下图所示。 
(1)除去粗盐中的Ca2+、Mg2+和SO42-,加入下列沉淀剂的顺序是(填序号)_________。
a. Na2CO3 b.NaOH c.BaCl2
(2)将滤液的pH调至酸性除去的离子是________________。
(3)电解饱和食盐水的离子方程式是_________________。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式
是_____________。
(5)纯碱在生产生活中有广泛的应用。
①纯碱可用于除灶台油污。其原因是(结合离子方程式表述)______________。
②常温下,向某pH =11的Na2CO3溶液中加入过量石灰乳,过滤后所得溶液pH=13。则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是___________。
③工业上,可以用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是_______________(已知碳酸的酸性强于次氯酸)。工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)路布兰法是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取、结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为____________________;
②硫酸钠和焦炭、石灰石反应的化学方程式为_______________ (已知产物之一为CaS);
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。
①图中的中间产物C是__________,D是________(写化学式);
②装置乙中发生反应的化学方程式为_____________________;
(3)联合制碱法是对氨碱法的改进,其优点是___________________;
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石等为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行?________________________
绿色化学是20世纪90年代出现的一个多学科交叉的研究领域。它可以诠释为环境友好化学,其核心内涵是反应过程和化工生产中,尽量减少或彻底消除使用和生产有害物质。
(1)下列各项符合“绿色化学”要求的是__________。
A.处理废弃物 B.治理污染点 C.杜绝污染源
(2)在我国西部大开发中,某省为筹建一大型化工基地,征集到下列方案,其中你认为合理的是____。
A.企业有权自主选择厂址
B.应建在水资源丰富、交通方便且远离城市的郊区
C.建在西部干旱区可以脱贫致富
D.不宜建在人口稠密的居民区
(3)山东海化集团纯碱厂是世界上最大的氨碱法纯碱生产企业和亚太地区最大的纯碱出口基地,其主要生产流程如下:
①从理论上看,循环生产是否需要再补充NH3?___________________
②从原料充分利用的角度看,该方法有两个明显的缺陷,分别是:a_________;b___________。我国化学家侯德榜改革国外的纯碱生产工艺,创造了侯德榜制碱法(又叫联碱法),生产流程可简要表示如下:
③该法与氨碱法的不同之处有两点,分别是:_________、_________
④从理论上看,每生产1 mol Na2CO3,需再补充的物质及其物质的量分别是_________。著名化学家侯德榜改革国外的纯碱生产工艺,发明的新生产流程可简要表示如下: 
(1)上述生产纯碱的方法称___,副产品的一种用途为___;
(2)沉淀池中发生的化学反应方程式是________;
(3)写出上述流程中X物质的分子式___;
(4)此流程能使原料氯化钠的利用率达到90%以上,主要是因为设计了循环____(填上述流程中的编号);
(5)从沉淀池中分离出沉淀的操作是___;
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加____。纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl2,请写出该工艺中产生CaCl2的化学方程式:___。
(2)写出“联合制碱法”有关反应的化学方程式:____。
(3)CO2是制碱工业的重要原料,“联合制碱法”中CO2的来源是___,“氨碱法”中CO2的来源是____。 (4)“联合制碱法”与“氨碱法”相比优点在于___。纯碱是工业生产的重要原料,很长一段时间内纯碱的制法被欧美国家所垄断。上个世纪初我国著名的化学家侯德榜先生,经过数年的反复研究终于发明了优于欧美制碱技术的联合制碱法(又称侯氏制碱法)。并在天津建造了我国独立研发的第一家制碱厂。其制碱原理的流程如下 
(1)侯德榜选择天津作为制碱厂的厂址有何便利条件:_________________ (举两例说明)。
(2)合成氨工厂需要向制碱厂提供两种原料气体,它们分别是____、____(填化学式)。这两种气体在使用过程中是否需要考虑添加的顺序?____(填“需要”或“不需要”),原因是_____________。
(3)在沉淀池中发生反应的化学方程式是______________。
(4)联合制碱法使原料水中溶质的利用率从70%提高到90%以上,主要是设计了_________(填上述流程中的编号)。从母液中提取出的副产品的应用是____________(举一例)。下图是合成氨和利用氨制取硝酸、纯碱的简要流程示意图: 
(1)设备A的名称是________,设备B的名称是___________。
(2)有关合成氨工业的说法中,正确的是__________(填序号)。
A.从合成塔出来的混合气体,其中NH3只占15%,所以生产氨的工厂的效率都很低
B.由于氨易液化,N2、H2是循环使用,所以总体来说氨的产率很高
C.合成氨工业的反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D.合成氨厂采用的压强是2×107~5×107Pa,因在该压强下铁触媒的活性最大
(3)在纯碱制造过程中,过程①与过程②的顺序能否颠倒?______(填“能”或“否”),为什么?________________________。若产品纯碱中含有碳酸氢钠,用加热分解的方法测定纯碱中碳酸氢钠的质量分 数,则其质量分数可表示为___________________________ (注明表达式中所用符号的含义)。
(4)硝酸厂的尾气中含有NO和NO2等污染物,常利用各种燃料气中的甲烷等将氮的氧化物还原为空气的主要成分而除去。写出甲烷与NO2反应的化学方程式:____________________。若基于下列反应的方法治理:2NO2+2NaOH=NaNO3+NaNO2+H2O,NO+NO2+2NaOH=2NaNO2+H2O;标准状况下NO、NO2的混合物恰好与50 mL 2.0 mol/L的NaOH溶液完全反应,且生成NaNO2和NaNO3的物质的量的比值为4:1,则在混合气体中NO的体积分数为_________。以食盐为原料进行生产并综合利用的某些过程如下图所示。 
(1)除去粗盐中的Ca2+、Mg2+和SO42-离子,加入下列沉淀剂的顺序是(填序号)_________。
a.Na2CO3 b.NaOH c.BaCl2
(2)将滤液的pH调至酸性除去的离子是_________。
(3)电解饱和食盐水反应的离子方程式是_________。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是_________。
(5)纯碱在生产生活中有广泛的应用。
① 纯碱可用于除灶台油污。其原因是(结合离子方程式表述)__________________。
② 常温下,向某pH=11的Na2CO3溶液中加入过量石灰乳,过滤后所得溶液pH=13。则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是_________。
③ 工业上,可以用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是__________________。(已知碳酸的酸性强于次氯酸)。根据侯德榜制减法原理并参考下表的数据,实验室制备纯碱Na2CO2的主要步骤是:将配制好的饱和NaCl溶液倒入烧杯中加热,控制温度在30-35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2小时,制得Na2CO3固体。 
①>35°NH4HCO3会有分解
请回答:
(1)反应温度控制在30-35℃,是因为若高于35℃则 ,若低于30℃,则________________________;为控制此温度范围,采取的加热方法为________________________。
(2)加料完毕后,继续保温30分钟,目的是________________________。静置后只析出NaHCO3晶体的原因是________________________。用蒸馏水洗涤NaHCO3晶体的目的是除去___________________杂质(以化学式表示)。
(3)过滤所得的母液中含有____________(以化学式表示),需加入________________,并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl。
(4)测试纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品Wg,放入锥形瓶中加蒸馏水溶解,加
1-2滴酚酞指示剂,用物质的量浓度为c(mol/L)的HCl溶液滴定至溶液由红色到无色(指示CO32-+H+=
HCO3-反应的终点),所用HCl溶液体积为V1mL,再加1-2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄变橙,所HCl溶液总体积为V2mL。写出纯碱样品中NaHCO3质量分数的计算式:NaHCO3(%)=
____________。氨碱法和侯氏制碱法的生产流程图可用如图表示,试回答下列问题。 
(1)请把图中的数字用具体的化学式表示:①___、②___、③___、④___。
(2)“氨碱法”产生大量的CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式:____;“侯氏制碱法”中,在母液中通入③的目的是________。
(3)CO2是制碱工业的重要原料,“侯氏制碱法”与“氨碱法”中CO2的来源有何不同:____。
(4)取“侯氏制碱法”生产的纯碱样品(设其中的杂质不与盐酸反应)11.0 g配成250.00 mL溶液,取25.00 mL溶液用1.00 mol.L-1的标准盐酸滴定,用酚酞作指示剂,三次滴定消耗盐酸的平均量为10.00 mL。请计算纯碱样品的纯度______。我国化学家侯德榜改革国外的制碱工艺提出的“侯氏制碱法”誉满全球。其生产步骤如下图所示: 
试完成下列问题:
(1)若上述的悬浊液是NaHCO3与NH4 Cl的混合物,则I和Ⅱ的总反应式是___________ 。
(2)由这一反应可知NaCl比NaHCO3溶解度____________。
(3)操作I、Ⅱ不能颠倒的原因是_____________。
(4)Ⅲ的操作叫__________;Ⅳ的操作叫_____________。三聚氰胺(化学式:C3N6H6)是一种非食品类的重要有机化工原料,广泛用于塑料、造纸、建材等行业。下图是我国科技工作者研制的以尿素为原料生产三聚氰胺的工艺——“常压气相一步法联产纯碱新技术”:
已知:①尿素的熔点是132.7℃,常压下超过160℃即可分解;
②三聚氰胺的熔点是354℃,加热易升华,微溶于水;
③以尿素为原料生产三聚氰胺的原理是:6 CO(NH2)2 C3N6H6 +6 NH3 + 3 CO2
C3N6H6 +6 NH3 + 3 CO2
请回答:
(1)尿素是一种常用含氮量最高的化肥,其氮元素的质量百分数为_________,在实验室使其熔化的容器名称叫_________ 。
(2)工业上合成尿素的化学反应方程式为___________________(反应条件可以不写)
(3)写出各主要成份的化学式:产品1______、产品2_________、X ________;
(4)联氨系统沉淀池中发生的化学反应方程式为:_____________;
(5)为了使母液中析出更多的产品2 ,常用的方法是____________
A、加入固体NaCl B、加入固体NaHCO3 C、通入CO2气体 D、通入NH3
(6)若生产过程中有4%的尿素损耗,每吨尿素可生产三聚氰胺________吨, 副产品纯碱__________吨。(精确到0.001)我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下 
(1) 上述生产纯碱的方法称___________,副产品的一种用途为___________。
(2) 沉淀池中发生的化学反应方程式是______________________。
(3) 写出上述流程中X物质的分子式___________。
(4) 使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 ___________(填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作是______________________。
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加___________。
(6) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有_________。
(a) 增大NH4+的浓度,使NH4Cl更多地析出
(b) 使NaHCO3更多地析出
(c) 使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度【三选一---化学与技术】
纯碱是工业生产的重要原料,很长一段时间内纯碱的制法被欧美国家所垄断。上个世纪初我国著名的化学家侯德榜先生,经过数年的反复研究终于发明了优于欧美制碱技术的联合制碱法(又称侯氏制碱法)。并在天津建造了我国独立研发的第一家制碱厂。其制碱原理的流程如下
(1)侯德榜选择天津作为制碱厂的厂址有何便利条件:_________________ (举两例说明)。
(2)合成氨工厂需要向制碱厂提供两种原料气体,它们分别是____、____(填化学式)。这两种气体在使用过程中是否需要考虑添加的顺序?____(填“需要”或“不需要”),原因是_____________。
(3)在沉淀池中发生反应的化学方程式是______________。
(4)联合制碱法使原料水中溶质的利用率从70%提高到90%以上,主要是设计了_________(填上述流程中的编号)。从母液中提取出的副产品的应用是____________(举一例)。【三选一----化学与技术】
纯碱是一种重要的化工原料,目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。请按要求回答问题:
(1)“氨碱法”产生大量CaCl2废弃物,请写出该工艺中产生CaCl2的化学方程式:___________;
(2)写出“联合制碱法”有关反应的化学方程式:___________ 、____________ ;
(3)CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同? _____________;
(4)“联合制碱法”是对“氨碱法”的改进,其相对优点有___________ (填序号)
A.提高了原料的原子利用率 B.降低了生产成本 C.减少了环境污染
D.减轻了对设备的腐蚀
(5)绿色化学的主要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:原子利用率(%)= ____________ 。
(6)产品纯碱中常含有碳酸氢钠,如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,已知所取产品的质量为m1g,加热后所剩固体的质量为m2g,则纯碱中碳酸氢钠的质量分数可表示为 _____________。【三选一化学与技术】
海水的综合利用,对于人类的生产生活有重要的意义。
(1)海水淡化沿海缺水地区获取淡水的方法之一,列举出海水淡化的两种方法_____________、________________。
(2)氯碱工业离子交换膜法生产中,透过离子交换膜的离子为_____________,氢氧化钠产生于____________(填‘“阳极”或“阴极”)。
(3)氯化钠为工业制纯碱的主要原料,制碱反应过程中法中析出NaHCO3的原因是______________;侯氏制碱法与索尔维制碱法相比除提高食盐利用率、无氯化钙生成的优势外还有______________ 、_______________ 从而综合利用原料、降低成本、减少环境污染。(三选一)【化学与技术】
纯碱一直以来都是工业生产的重要原料,很长一段时间纯碱的制法都被欧美国家所垄断。上个世纪初,我国著名的工业化学家侯德榜先生经过数年的反复研究终于发明了优于欧美制碱技术的联合制碱法(又称侯氏制碱法)。并在天津建造了我国独立研发的第一家制碱厂。其制碱原理的流程如图
(1)侯德榜选择天津作为制碱厂的厂址有何便利条件(举二例说明):______、_____。
(2)合成氨工厂需要向制碱厂提供两种原料气体,它们分别是 ____、____(填化学式);这两种气体在使用过程中是否需要考虑添加的顺序:____(填“是”或“否”),原因是____________________。
(3)在沉淀池中发生的反应的化学方程式:________________。
(4)使原料水中溶质的利用率从70%提高到90%以上,主要是设计了__________(填上述流程中的编号)。从母液中可以提取的副产品的应用是____________(举一例)。工业上以粗食盐(含有少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3。其过程如下图所示。 
请回答:
(1)在处理粗盐水的过程中,可加入石灰乳和纯碱作为沉淀剂,则所得滤渣的成分除过量的沉淀剂外还有_____________。
(2)将CaO投入含有大量的NH4Cl的母液中,能生成可循环使用的NH3,该反应的化学方程式是_________________。
(3)向饱和食盐水中首先通入的气体是______,过程Ⅲ中生成NaHCO3晶体的反应的化学方程式是__________________。
(4)碳酸钠晶体失水的能量变化示意图如下:
Na2CO3·H2O(s) 脱水反应的热化学方程式是___________。
(5)产品纯碱中常含有NaCl。取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体。则该产品中Na2CO3的质量分数是__________。
(6)熔融Na2CO3可作甲烷--空气燃料电池的电解质,该电池负极的反应式是________________________。[三选一选修2:化学与技术]
NaCl是价廉且应用广泛的化工业原料,例如,纯碱工业、氯碱工业、氯酸钾工业、肥皂工业等。
(1)19世纪60年代氨碱法是纯碱工业广泛使用的方法,20世纪20年代以后被联合制碱法逐渐取代。
①请写出以NaCl为原料利用氨碱法生产纯碱的化学方程式_______ ;
②在联合制碱法中,纯碱工厂与__________工厂进行联合生产,以方便的获得原料____________ ;
③在联合制碱法中循环使用,而在氨碱法中循环使用率不高的物质是____________。
(2)氯酸钾是重要的化工业产品,在火柴、炸药、雷管、焰火等制造中有重要应用,工业中首先通过电解热食盐水制得氯酸钠,再加入一定量的氯化钾即可得到氯酸钾沉淀。
①在火柴、炸药、雷管、焰火的制造过程中大量使用氯酸钾,主要应用氯酸钾的_________性;
②请写出电解食盐水生产氯酸钠的化学方程式___________,该工艺过程中使用的装置与氯碱工业中使用的装置主要区别有______________(请答出两点);
(3)在肥皂的工业生成过程中,也要使用NaCl的目的是___________。工业生产纯碱的工艺流程示意图如下 
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式.
A.________,B.________.
(2)实验室提纯粗盐的实验操作依次为:取样、________、沉淀、________、________、冷却结晶、________、烘干.
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是________________.碳酸化时没有析出碳酸钠晶体,其原因是________________________.
(4)碳酸化后过滤、滤液D最主要的成分是________________(填写化学式),检验这一成分的阴离子的具体方法是:________________________________.
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨.加石灰水后所发生的反应的离子方式程为:________________________________,滤液D加石灰水前先要加热,原因是________________.
(6)产品纯碱中含有碳酸氢钠.如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:________________________.“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”是著名的“侯氏制碱法”的重要反应.下面是4位同学对该反应涉及的有关知识发表的部分见解.其中不正确的( ) A. 
B. 
C. 
D. 
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献.他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱.有关反应的化学方程式为:
NH3+CO2+H2O=NH4HCO3;
NH4HCO3+NaCl=NaHCO3↓+NH4Cl;
2NaHCO3
Na2CO3+CO2↑+H2O△ .
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是______
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验.
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出).
试回答下列有关问题:
(Ⅰ)乙装置中的试剂是______;
(Ⅱ)丁装置中稀硫酸的作用是______;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是______(填分离操作的名称).
②另一位同学用图中戊装置(其它装置未画出)进行实验.
(Ⅰ)实验时,须先从______管通入______ 气体,再从______管中通入______气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是______;
(3)请你再写出一种实验室制取少量碳酸氢钠的方法:______.我国著名的化工专家侯德榜在20世纪20年代所创立的“侯氏制碱法”誉满全球.“侯氏制碱法”中的碱是指下列的( ) A.NaOH B.K2CO3 C.Na2CO3 D.NaHCO3 我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下: 
(1)上述生产纯碱的方法称______,副产品的一种用途为______.
(2)沉淀池中发生的化学反应方程式是______.
(3)写出上述流程中X物质的分子式______.
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了______(填上述流程中的编号)的循环.从沉淀池中取出沉淀的操作是______.
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加______.符合实际并用于工业生产的是( ) A.CO2通入氢氧化钠溶液中制Na2CO3 B.H2和Cl2光照制HCl C.Cl2通入澄清石灰水中制漂粉精 D.用硫磺制硫酸 纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域.工业上以食盐、氨气(主要由合成氨厂提供)和二氧化碳为主要原料生产纯碱.其流程如下:根据以上信息回答下列问题.
(1)盐水精制的过程是除去溶液中各种杂质的过程.为将盐水中含有的Ca2+、Mg2+等沉淀,可以向其中加入过量纯碱.此时将混合液中不溶物除去的方法是______;溶液中多余的纯碱可以加______试剂来除去.
(2)上述工艺流程中,加压条件下通入二氧化碳进行碳酸化时没有析出碳酸钠晶体,其原因是______.
(3)在氨碱工业的历史上,如何处理流程中剩余的滤液,出现了两种工艺:一是“索尔维法”,即在滤液中加入石灰水;二是我国化学家侯德榜发明的“联合制碱法”,即在滤液中加入适量氯化钠晶体.
①“索尔维法”中,滤液加石灰水前先要加热,原因是______.
②“联合制碱法”中,可以循环利用的物质是______ (用化学式表示).
(4)若采用上述流程生产106吨纯碱,则理论上通入的二氧化碳的体积(标准状况下)不得少于______L(不考虑二氧化碳的回收利用).
我国化学家候德榜早在1929年改进了一种化工产品的生产技术,其产品获美国费城万国博览会金奖,这种生产技术是( ) A.烧碱生产 B.纯碱生产 C.粗盐精制 D.尿素生产 我国化学家侯德榜改革国外的Na2CO3生产工艺,创造了侯氏制碱法,又叫联邦制碱法,该法是将合成氨工厂生产的NH3及副产品
CO2,通入到饱和食盐水中得到NaHCO3,分离出的NaHCO3加热制得Na2CO3.某研究性学习小组设计如图所示的模拟装置,该装置可实现部分原料的循环使用.
(1)分液漏斗甲中为盐酸,装置B中试剂为______,分液漏斗乙中是易挥发的某试剂,该试剂为______.
(2)实验操作过程中,应先打开______(填“k1”或“k2”),当观察到______现象时,再打开另一个弹簧夹.
(3)装置E中试剂为饱和NaCl溶液,该装置能体现绿色化学思想的两个作用是______、______.
(4)老师认为在C、D之间还应增加一个装置,该装置作用为______.
(5)写出C中生成NaHCO3的化学方程式______.已知NaHCO3低温时溶解度小,侯德榜制碱的方法是:向氨化的饱和食盐水中通入过量的二氧化碳,即有晶体析出,经过滤、洗涤、焙烧得纯碱.此过程可以表示为:
①NaCl (饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl(此反应是放热反应)
②2NaHCO3
Na2CO3+CO2↑+H2O△ .
现某化学小组根据上述原理在实验室中模拟制碱过程,下图C装置是溶有氨和NaCl的溶液,且二者均达到了饱和.
(1)制CO2时为了使反应随开随用,随关随停,上图A方框内应选用以下______装置.简述该装置随关随停的理由______.
(2)为使实验能够进行,在B、D方框内补上所需装置,并指明所用试剂(将装置图画在答题纸上)
(3)完成第(2)步,该小组检验气密性合格后进行实验,发现析出的晶体非常少,在老师的指导下,他们对某个装置进行了改进,达到了实验目的.你认为他们的改进方法是______.
(4)若所用饱和食盐水中含有NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.46g,假设第二步分解时没有损失,则Na2CO3的产率为______.1942年中国科学家侯德榜发明了举世闻名的“侯氏制碱法”,成为世界上生产纯碱的重要方法.其主要化学原理是:NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3;2NaHCO
Na2CO3+H2O+CO2↑.该原理中体现了NaHCO3的什么性质( )△ . A.酸性 B.碱性 C.水溶性 D.热不稳定性
- A: _____ mask is it? B: Sorry, I don"t know. [
- 如图,正方形ABCD的面积为1,M 是AB的中点,则图中阴影部分的面积是[ ]A.B.C.D.
- You ________ your son to watch TV for too long hours! See,
- 下列说法正确的是A.1mol任何气体的体积都约是22.4 LB.20℃,1.0×105Pa,同体积的O2,CO2含有相同
- 化学与生活密切相关,请你用所学化学知识回答以下问题:⑴家庭使用的燃料,大多是罐装液化石油气,其主要成分有丙烷(化学式为C
- 在区间[-π6,π2]上随机取一个数x,则sinx+cosx∈[1,2]的概率是( )A.12B.34C.38D.58
- 7x-3-5x+2=______.
- 用圆规和直尺作图,不写作法,但要保留作图痕迹已知:如图∠AOB求作:以OA为边的∠AOC,使∠AOC=12∠BOC.
- 下列各式中是最简二次根式的是[ ]A.B.C.D.
- 如图,D,E为等边△ABC的边AB,BC的中点,则与△ABE全等的三角形有 [ ]A.1个 B.2个 C
- 下列有关天气预报的叙述,正确的是( )A.天气预报要说明某地一日内冷暖情况B.天气预报的内容通常包括阴、晴、风、气温和
- Einstein liked Bose’s paper so much that he ________ his own
- (3分)我市五通桥区有丰富的盐卤资源,是我国有名的井盐产地。下面是以井盐水为原料生产食盐及利用食盐生产某些化工产品的流程
- 草履虫的细胞内没有______不能自己制造有机物。
- 1997年7月1日香港维多利亚港湾的会展中心灯火辉煌,0时整,伴随着嘹亮的中华人民共和国国歌,鲜艳的五星红旗冉冉升起。从
- 为测定其碳酸钙的含量标注是否属实,现取出4片片剂,研碎后放入烧杯中,逐滴加入一定量稀盐酸,恰至不再放出气体为止,化学方程
- ‘你幸福吗?”、“航母style”、“打铁还须自身硬”、“钓鱼岛是中国的”… … 等2012年网络语的出现和流行,反映出
- 下列科学家属于英国的有①牛顿②达尔文③爱因斯坦④哥白尼[ ]A.①③B.②④C.①②D.③④
- 近年来,台商在珠江三角洲地区的投资开始减少,其原因可能是[ ]A.交通不便B.生产成本上涨C.自然条件差D.政策
- 下图表示某地7月份某一天的气温随时间变化的情况,请观察此图,并回答下列问题:(1)这天的最高气温是( )℃;(2)
© 2017-2019 超级试练试题库,All Rights Reserved.