中和滴定实验
酸碱中和滴定
用已知物质的量浓度的酸(或碱)来测 定未知物质的量浓度的碱(或酸)的方法叫做酸碱中和滴定。
(1)原理:对于一元酸和一元碱发生的中和反应,C酸V酸=C碱V碱 或:C未知V未知=C标准V标准,
(2)仪器:a.酸式滴定管 b.碱式滴定管c.铁架台d.滴定管夹e.锥形瓶 f.烧杯g.胶头滴管等
(3)装置图:
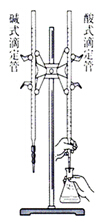
(4)操作步骤:
洗涤、检漏、水洗、润洗、装液、去泡、调液面记录、放待测液、加指示剂、滴定、记录、
计算、误差分析
(5)数据处理依据:
c(NaOH)=c(HCl)V(HCl)/V(NaOH)
(6)误差分析:
①仪器润洗不当:
a.盛标准液的滴定管用蒸馏水洗后未用标准液润洗;
b.盛待测液滴定(移液)管用蒸馏水洗后未用待测液润洗;
c.锥形瓶用蒸馏水洗后再用待测液润洗;
②读数方法有误:
a.滴定前仰视,滴定后俯视;
b.滴定前俯视,滴定后仰视;
c.天平或量筒的使用读数方法错误;
③操作出现问题:
a.盛标准液的滴定管漏液;
b.盛待测液的滴定管滴前尖嘴部分有气泡,终了无气泡
(或前无后有);
c.振荡锥形瓶时,不小心有待测液溅出;
d.滴定过程中,将标准液滴到锥形瓶外;
中和滴定中的误差分析
中和滴定是一个要求较高的定量实验,每一个不当的或错误的操作都会引起误差。
对于一元酸与一元碱,由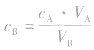 可知,VB是准 确量取的体积,CA标准溶液的浓度,它们均为定值,所以CB的大小取决于VA的大小,VA大则CB大,VA小则CB小。
可知,VB是准 确量取的体积,CA标准溶液的浓度,它们均为定值,所以CB的大小取决于VA的大小,VA大则CB大,VA小则CB小。
以标准酸溶液滴定末知浓度的碱溶液(酚酞作指示剂)为例,常见的不正确操作对实验结果的影响见下表:
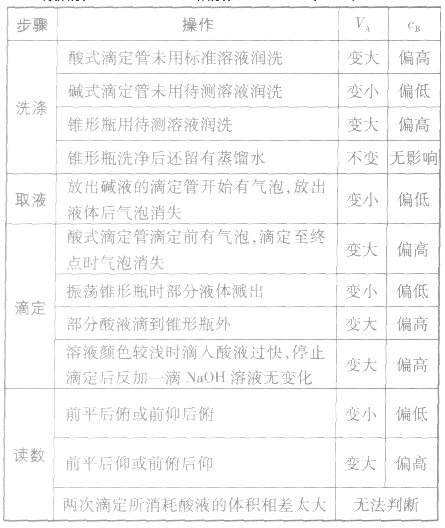
中和滴定应注意的问题
1.中和滴定中指示剂的使用与选择
(1)用量不能太多,常用2~3滴,冈指示剂本身也是有机弱酸或有机弱碱,若用量太多,会使中和滴定中需要的酸或碱的量增多或减少。
(2)指示剂的选择:中和滴定时一般选用的指示剂有酚酞和甲基橙。石蕊试液由于颜色变化不明显,不易辨别,在滴定过程中不宜使用。
(3)酸、碱恰好完全反应时,终点溶液的pH应在指示剂的变色范围内,如强酸溶液滴定弱碱溶液应选用甲基橙作指示剂;强碱溶液滴定弱酸溶液应选用酚酞作指示剂。
(4)指示剂的变色:最好由浅到深,这样对比明显。如用强碱滴定强酸用酚酞作指示剂较好,当酚酞从无色变为粉红色(或浅红色)且半分钟内不褪色时即达到滴定终点。
2.欲减小实验误差的三点做法
(1)半分钟:振荡,半分钟内颜色不褪去,即为滴定终点。
(2)l一2min:滴定停止后,必须等待l~2min,让附着在滴定管内壁的溶液流下后,再进行读数。
(3)重复:同一实验,要做两到三次,两次滴定所用标准溶液的体积的差值不能超过0.02mL,再取平均值。
用一定物质的量浓度的NaOH溶液滴定10mL一定物质的量浓度的盐酸,有关关系如图所示,据图推出
NaOH溶液和盐酸的物质的量浓度是
[ ] C(HC1)(mol·L-1) C(NaOH)(mol·L-1)
A. 0.12 0.04
B. 0.04 0.12
C. 0.18 0.06
D. 0.09 0.03(1)根据下列仪器回答问题:
A、容量瓶 B、蒸馏烧瓶 C、滴定管 D、量筒 E、烧杯 F、蒸发皿 G、分液漏斗
①有温度标志的有_________(填序号);
②使用时必须检查是否漏水的有____________(填序号);
③对允许加热的仪器,加热时必须垫上石棉网的有____________(填序号);
(2)现用物质的量的浓度为amol / L的标准NaOH溶液去测定VmL盐酸的物质的量浓度,下图是碱式滴定管中液面在滴定前后的读数:
c(HCl)=_______________ 用标准盐酸溶液滴定未知浓度的氢氧化钠溶液,如果测得结果偏低,则产生误差的原因可能是下列叙述中的 [ ] A.锥形瓶用蒸馏水洗净后,未经干燥即进行滴定
B.滴定前酸式滴定管尖嘴部分有气泡,滴定终止时气泡消失
C.酸式滴定管未用标准盐酸溶液润洗
D.把氢氧化钠待测液移入锥形瓶中时,有少量碱液溅出实验室现有3种酸碱指示剂,其pH变色范围如下甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0 用
0.10 mol/L NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是[ ] A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂用已知浓度的盐酸滴定未知浓度的NaOH溶液,选用酚酞作指示剂,下列操作会导致测定结果偏低的是 [ ]
A.酸式滴定管未润洗就装标准液滴定
B.锥形瓶未用待测液润洗
C.读取标准液读数时,滴前仰视,滴定到终点后俯视
D.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,反应如下:
KHC8H4O4+NaOH=KNaC8H4O4+H2O。邻苯二甲酸氢钾溶液呈酸性,滴定到达终点时,溶液的pH约为9.1。
(1)为标定NaOH溶液的浓度,准确称取一定质量的邻苯二甲酸氢钾(KHC8H4O4)加入250mL锥形瓶中,加入适量蒸馏水溶解,应选用_____________作指示剂,到达终点时溶液由______色变为_______色,且半分钟不褪色。(提示:指示剂变色范围与滴定终点pH越接近误差越小。)
(2)在测定NaOH溶液浓度时,有下列操作:
①向溶液中加入1~2滴指示剂;
②向锥形瓶中加20mL~30mL蒸馏水溶解;
③用NaOH溶液滴定到终点,半分钟不褪色;
④重复以上操作;
⑤准确称量0.4000g~ 0.6000g邻苯二甲酸氢钾加入250mL锥形瓶中;
⑥根据两次实验数据计算NaOH的物质的量浓度。
以上各步操作中,正确的操作顺序是________________________________。
(3)上述操作中,将邻苯二甲酸氢钾直接放在锥形瓶中溶解,对实验是否有影响? ______________。(填“有影响”或“无影响”)
(4)滴定前,用蒸馏水洗净碱式滴定管,然后加待测定的NaOH溶液滴定,此操作使实验结果________。(填“偏大”“偏小”或“无影响”)
(5)现准确称取KHC8H4O4(相对分子质量为204.2)晶体两份各为0.5105g,分别溶于水后加入指示剂,用NaOH溶液滴定至终点,消耗NaOH溶液体积平均为20.00mL,则NaOH溶液的物质的量浓度为___________。(结果保留四位有效数字)实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,反应如下:
KHC8H4O4+NaOH=KNaC8H4O4+H2O。邻苯二甲酸氢钾溶液呈酸性,滴定到达终点时,溶液的pH约为9.1
(1)为标定NaOH溶液的浓度,准确称取一定质量的邻苯二甲酸氢钾(KHC8H4O4)加入250mL锥形瓶中,加入适量蒸馏水溶解,应选用_____________作指示剂,到达终点时溶液由______色变为_______色,且半分钟不褪色。(提示:指示剂变色范围与滴定终点pH越接近误差越小。)
(2)在测定NaOH溶液浓度时,有下列操作:
①向溶液中加入1~2滴指示剂;
②向锥形瓶中加20mL~30mL蒸馏水溶解;
③用NaOH溶液滴定到终点,半分钟不褪色;
④重复以上操作;
⑤准确称量0.4000g~0.6000g邻苯二甲酸氢钾加入250mL锥形瓶中;
⑥根据两次实验数据计算NaOH的物质的量浓度。
以上各步操作中,正确的操作顺序是_____________________。
(3)上述操作中,将邻苯二甲酸氢钾直接放在锥形瓶中溶解,对实验是否有影响? ______________。(填“有影响”或“无影响”)
(4)滴定前,用蒸馏水洗净碱式滴定管,然后加待测定的NaOH溶液滴定,此操作使实验结果________。(填“偏大”“偏小”或“无影响”)
(5)现准确称取KHC8H4O4(相对分子质量为204.2)晶体两份各为0.5105g,分别溶于水后加入指示剂,用NaOH溶液滴定至终点,消耗NaOH溶液体积平均为20.00mL,则NaOH溶液的物质的量浓度为___________。(结果保留四位有效数字)某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶
2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准硫酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入甲基橙作指示剂,进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗硫酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL蒸馏水,测得所耗硫酸为V2mL。
试回答下列问题:
(1)锥形瓶中的溶液从_______色变为_______色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察______________(填序号)
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)上述操作步骤中两处错误分别是______________,______________(请指出具体错误)。由此造成的测定结果分别是_______,_______(填偏高、偏低或无影响)。
(4)某次滴定时的滴定管中的液面如图,则其读数为_______mL。若记录读数时,起始时俯视,终点时仰视,则所测溶液浓度会_______(填偏高、偏低或无影响)。
(5)根据下列数据 
请计算待测烧碱溶液的浓度为______________mol/L。 某学生欲用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,判断滴定终点的方法为_____________________________________________
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗 净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:则起始读数为_________mL,终点读数
_____________mL;
(4)某学生根据三次实验分别记录有关数据如下 
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=______________。 某学生用物质的量的浓度为amol/L的标准NaOH去测定VmL HCl溶液的物质的量浓度。
回答下列问题:
(1)实验前应先检查滴定管_____________,实验过程中眼睛_________________;
(2)其操作可分解为如下几步:
A.取V/4mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液;
B.用标准氢氧化钠溶液润洗滴定管2~3次;
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2~3mL处;
E.调节液面至“0”至“0”刻度以下,记下读数;
F.把锥形瓶放在滴定管的下面,用标准氢氧化钠溶液滴定至终点并主下滴定管的读数。
正确的操作顺序是:_____、D 、 _____、 _____、 A、____ ;
(3)滴定至终点时的现象是:_____________________
(4)下图是碱式滴定管中液面在滴定前后的读数:
c (HCl) = ___________________。
(5)下列操作会使测定的HCl物质的量浓度偏大的是____________
A、滴定前碱式滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失;
B、滴定终点后溶液颜色迅速消失;
C、滴定前仰视,滴定终了平视;
D、实验前先用待测液润洗锥形瓶;
E、碱式滴定管用蒸馏水洗净后,未用标准溶液润洗,使滴定结果;常温下,用0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L HCl溶液,滴定曲线,如图所示。下列说法不正确的是 
[ ] A.a=20.00
B.滴定过程中,可能存在:c(Cl-)>c(H+)>c(Na+)>c(OH-)
C.若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定
D.若将盐酸换成同浓度的醋酸,则滴定到pH=7时,a>20.00I.如图1为向25mL 0.1mol·L-1NaOH溶液中逐滴滴加0.2mol·L-1CH3COOH溶液过程中溶液pH的变化曲线。请回答 
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?
________(选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?
________区间(若正确,此问不答)。
(2)关于该滴定实验,从下列选项中选出最恰当的一项________(选填字母)。
(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是________。
A.c(OH-)大于c(CH3COO-)
B.c(OH-)小于c(CH3COO-)
C.c(OH-)等于c(CH3COO-)
D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)________2c(Na+)(填“>”“<”或“=”)。
Ⅱ.t℃时,某稀硫酸溶液中c(H+) =10-amol·L-1,c(OH-) =10-bmol·L-1,已知a+b=13
(5)该温度下水的离子积常数Kw的数值为________。
(6)该温度下(t℃),将100mL 0.1mol·L-1的稀H2SO4与100mL 0.4mol·L-1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=________。现有常温条件下的甲、乙、丙三种溶液。甲为0.1mol·L-1的NaOH溶液,乙为 0.1mol·L-1的HCl溶液,丙为0.1mol·L-1的CH3COOH溶液,试回答下列问题
(1)乙溶液中,由水电离出的c(H+)=____________ mol·L-1;
(2)丙溶液中存在的电离平衡为________________________________(用电离平衡方程式表示);
(3)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为____________;
(4)某同学用甲溶液分别滴定20.00mL乙溶液和20.00mL丙溶液,得到如图所示两条滴定曲线,请完成有关问题
①甲溶液滴定丙溶液的曲线是_____________(填“图1”或“图2”);
②a=____________mL。常温下,用 0.1000mol·LNaOH溶液滴定20.00mL0.1000mol·L CH3COOH溶液所得滴定曲线如图。下列说法正确的是 
[ ] A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:c(Na+)=c(CH3COOH)+ c(CH3COO-)
C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)常温下,用0.1000mol/LNaOH溶液滴定20.00mL0.1000mol/LCH3COOH溶液所得滴定曲线如图。下列说法正确的是 
[ ] A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-)
C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)将某一元酸HA与NaOH等体积混合,请根据题目要求回答下列问题:
(1)若c(HA)=c(NaOH)=O.lmol/L,测得混合后溶液的pH>7。
①HA是弱电解质,能证明HA是弱电解质的方法是________________。
A.测得0.1mol/L HA的pH>l
B.测得NaA溶液的pH>7
C.pH=l的HA与盐酸,稀释10倍后,盐酸的pH变化大
D.用足量的锌分别与相同pH、相同体积的盐酸和HA反应,产生氢气一样多
②混合溶液中,关系式一定正确的是___________。
A.c(A-)>c(Na+)c(OH-)>c(H+)
B.c(A-)+c(OH-)=c(Na+)+c(H+)
C.c(HA)+c(A-)=0.1mol/L
D.c(HA) +c(H+)= c(OH-)
③若HA(足量)+B2-==A-+HB-;H2B(少量)+2C-==B2-+2HC;HA+C-==A-+HC
则相同pH的①NaA②Na2B③NaHB④NaC的四种溶液,各物质的物质的量浓度从大到小的顺序为___________(填序号)。
(2)若c(HA)==c(NaOH)==0.1mol/L,测得混合后溶液的pH=7。
①现将一定浓度的HA稀释10倍后溶液的pH与该浓度的HA和0.1mol/L NaOH等体积混合后溶液的pH相等,则HA溶液的浓度为____________。
②用标准的NaOH溶液滴定未知浓度的HA时,下列操作能引起所测HA浓度偏低的是______________。
A.用蒸馏水洗涤锥形瓶后,用待测HA溶液进行润洗
B.滴定前发现滴定管的尖嘴部分有气泡,滴定后消失
C.装NaOH的碱式滴定管未用标准的NaOH溶液润洗
D.滴定前仰视,滴定后俯视读数某学生用物质的量的浓度为amol/L的标准NaOH去测定VmL HCl溶液的物质的量浓度。回答下列问题: (1)实验前应先检查滴定管__________________,实验过程中眼睛__________________;
(2)其操作可分解为如下几步:
A.取V/4 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液;
B.用标准氢氧化钠溶液润洗滴定管2~3次;
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2~3mL处;
E.调节液面至“0”至“0”刻度以下,记下读数;
F.把锥形瓶放在滴定管的下面,用标准氢氧化钠溶液滴定至终点并主下滴定管的读数;
正确的操作顺序是:___ 、D 、 _____ 、 _____、 A、____ ;
(3)滴定至终点时的现象是:_____________________
(4)下图是碱式滴定管中液面在滴定前后的读数
c (HCl) =__________________
(5)下列操作会使测定的HCl物质的量浓度偏大的是________________
A、滴定前碱式滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失;
B、滴定终点后溶液颜色迅速消失;
C、滴定前仰视,滴定终了平视;
D、实验前先用待测液润洗锥形瓶;
E、碱式滴定管用蒸馏水洗净后,未用标准溶液润洗,使滴定结果;用0.10mol/L的NaOH溶液滴定100.0mL0.10mol/LHCl溶液时,滴定误差在±0.1%以内,反应完毕后溶液的pH变化范围是 [ ] A.6.9~7.1
B.4.3~9.7
C.3.6~10.4
D.以上都不正确在化学实验操作中,往往由于读数不规范导致较大的实验误差。下列有关实验中,会导致所配制(或所测定)溶液浓度偏大的是(其他操作均正确) [ ] A.配制500mL 1mol/L稀硫酸实验中,用量筒量取18.1mol /L浓硫酸时俯视读数
B.配制1mL 5.1mol/L氯化钠溶液实验中,定容时仰视
C.用标准盐酸滴定特测NaOH溶液实验中,使用碱式滴定管开始平视,后来俯视读数
D.用标准NaOH溶液滴定特测盐酸实验中,使用碱式滴定管开始平视,后来俯视读数某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定。下表是4种常见指示剂的变色范围 
(1)该实验应选用________作指示剂,向锥形瓶中移取一定体积的白醋所用的仪器是__________。
(2)下图表示50mL,滴定管中液面的位置,若A与C刻度间相差1mL, A处的刻度为25,滴定管中液面读数应为_____________mL。此时滴定管中液体的体积_____________。
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准漓浓度为c mol·L-1,三次实验结果记录如下 
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是________。
A.实验结束时俯视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
E.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)根据所给数据,写出计算该白醋中总酸度的表达式(不必化简):__________________________。在一支25 mL的酸式滴定管中盛入0.1 mol·L-1 HCI溶液,其液面恰好在5 mL的刻度处,若把滴定管中的溶液全部放入烧杯中,然后以0.l mol·L-1 NaOH溶进行中和,则所需NaOH溶液的体积 [ ] A.大于20 mL
B.小于20 mL
C.等于20 mL
D.等于5mL实验室现有3种酸碱指示剂,其pH变色范围如下:甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0用0.1000 mol·L-1 NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是 [ ] A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定,在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_____。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸、润洗
C.锥形瓶水洗后未干燥
D.碱式滴定管尖嘴部分有气泡,滴定后消失在中和滴定实验中,下列操作不影响测定结果的是 [ ] A.滴定管用蒸馏水洗净后,直接装滴定液
B.锥形瓶用蒸馏水洗净后,再用待测液润洗
C.滴定过程中,锥形瓶里的液体溅到瓶外
D.用蒸馏水冲洗附在锥形瓶内壁上的液滴某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
② 固定好滴定管并使滴定管尖嘴充满液体
③ 调节液面至“0”或“0”刻度线稍下,并记下读数
④ 移取20.0mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤ 用标准液滴定至终点,记下滴定管液面读数。
请回答
(1)以上步骤有错误的是(填编号)____________,该错误操作会导致测定结果 (填“偏大”、“偏小”或“无影响”)_______________
(2)判断滴定终点的现象是:锥形瓶中溶液从_______色变为_______色,且半分钟不变色
(3)上图是某次滴定时的滴定管中的液面,其读数为_______mL
(4)根据下列数据:请计算待测盐酸溶液的浓度:_______mol/L
用0.01mol·L-1 H2SO4滴定0.01mol·L-1NaOH溶液,中和后加水至100mL。若滴定时终点判断有误差:
①多加了1滴H2SO4;②少加了1滴H2SO4(设1滴为0.05mL)。则①和②C(H+)之比的值为[ ] A.10
B.50
C.5×103
D.104已知常温常压下,饱和CO2溶液的PH=3.9,当用盐酸滴定NaHCO3溶液以测定其浓度时,选用的指示剂及终点颜色变化是 [ ] A.石蕊,蓝变红
B.酚酞,红色褪去
C.甲基橙,橙变黄
D.甲基橙,黄变橙用已知浓度的盐酸来测定某Na2CO3溶液的浓度时,若配制Na2CO3溶液时所用Na2CO3中分别含有:
①NaOH②NaCl③NaHCO3④K2CO3杂质,所测结果偏低的是[ ] A.仅①
B.仅②
C.仅②③
D.②③④当用酸滴定碱时,下列操作使测定结果(碱的浓度)偏高的是 [ ] A.酸式滴定管滴至终点,俯视读数
B.碱液移入锥形瓶后,加入10mL蒸馏水
C.酸式滴定管注入酸溶液后,尖嘴有气泡时便开始滴定,滴定后没气泡
D.酸式滴定管用蒸馏水润洗后,未用标准液润洗甲、乙两同学进行化学研究性学习:测定某次雨水的pH并判断某次雨水是否为酸雨。
甲同学取pH试纸用蒸馏水湿润后置于表面皿中,取雨水少量并滴几滴雨水到pH试纸上,稍许,与标准比色卡对照,测得pH为6。由此,甲同学得出这次雨水不是酸雨的结论。
乙同学用烧杯取雨水少许,用pH试纸正确测定该雨水的pH,测得pH为5。露置于教室中一段时间后,再测得pH为4。
请回答下列问题:
(1)甲、乙两同学上述化学研究性学习思路的可取之处是_________________________。
(2)你认为甲同学的结论是否合理并说明你的理由_________________________。
(3)请你解释乙同学的实验中先测得pH为5,露置于教室中一段时间后,再测得pH为4的原因(用化学方式式并结合文字说明)__________________________
(4)酸雨形成的原因与下列那些气体有关________(填代号)
A:CO2 B:SO2 C:CO D:NO2已知c(NH4Cl)<0.1 mol·L-1时,溶液的pH>5.1,现用0.1 mol·L-1盐酸滴定10mL 0.05mol·L-1氨水,用甲基橙作指示剂,达到终点时所用盐酸的量应是 [ ] A.10mL
B.5mL
C.大于5mL
D.小于5mL用标准盐酸滴定未知浓度的NaOH溶液,下列各操作中不会引起实验误差的是 [ ] A.用蒸馏水洗净酸式滴定管后,装入标准盐酸后立即进行滴定
B.用蒸馏水洗净锥形瓶后,再用待测的NaOH溶液润洗而后装入一定体积的NaOH溶液进行滴定
C.用碱式滴定管取20.00mL NaOH溶液放入用蒸馏水洗净的锥形瓶中再加入适量蒸馏水进行滴定
D.将用标准液润洗后的酸式滴定管关闭活塞,加标准液刚好至“0”刻度线,将锥形瓶移至滴定管下,进行滴定常温下,用0.1000 mol·LNaOH溶液滴定20.00mL 0.1000 mol·LCH3COOH溶液所得滴定曲线如图。下列说法正确的是 
[ ] A.点①所示溶液中:C(CH3COO-)+C(OH-)=C(CH3COOH)+ C(H+)
B.点②所示溶液中:C(Na+)=C(CH3COOH)+ C(CH3COO-)
C.点③所示溶液中:C(Na+)>C(OH-) >C(CH3COO-) >C(H+)
D.滴定过程中可能出现:C(CH3COOH) >C(CH3COO-) >C(H+)>C(Na+)>C(OH-)某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250 mL 0.2 mol/L的醋酸溶液,用0.2 mol/L的醋酸溶液稀释成所需浓度的溶液,再用
NaOH标准溶液对所配醋酸溶液的浓度进行标定。
回答下列问题:
(1)配制250mL 0.2mol/L 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、______________和
_______________。
(2)为标定某醋酸溶液的准确浓度,用0.2000mol/L的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下
则该醋酸溶液的准确浓度为_____________。(保留小数点后四位)
实验二 探究浓度对醋酸电离程度的影响用pH计测定25℃时不同浓度的醋酸的pH,其结果如下
回答下列问题:
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是______________。
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度___________。(填增大、减小或不变)
实验三 探究温度对醋酸电离程度的影响
(5)请你设计一个实验完成该探究,请简述你的实验方案
_______________________________实验室现有3种酸碱指示剂,其pH变色范围如下
甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0
用0.1000mol/L NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是[ ] A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂测血钙的含量时,可将2.0mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀。将沉淀用稀硫酸处理得H2C2O4后,再用KMnO4某酸性溶液滴定,氧化产物为CO2,还原产物为Mn2+,若终点时用去20.0 mL 1.0×10-4 mol·L-1的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式_________________________。
(2)判断滴定终点的方法是__________________________________。
(3)计算:血液中含钙离子的浓度为__________________g·mL-1。下列各表述与示意图一致的是 
[ ] A.图①表示25℃时,用0.1mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2(g) + O2(g) 2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化
C.图③表示10mL 0.01mol·L-1 KMnO4酸性溶液与过量的0.1mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2(g) + H2(g)→CH3CH3(g);ΔH<0使用和未使用催化剂时,反应过程中的能量变化准确移取25.00mL某未知浓度的盐酸溶液于一洁净锥形瓶中,然后用0.20mol/L NaOH溶液滴定(指示剂为酚酞)。滴定结果如下 
(1)根据以上数据可计算出盐酸的物质的量浓度为____________mol/L(精确到0.01)。
(2)锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积_________(填“偏大”、“偏小”或“无影响”)
(3)滴定时边滴边摇动锥形瓶,眼睛应观察_____________
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(4)达到滴定终点的标志是_________________
(5)若操作有误,则导致待测盐酸溶液浓度偏低的错误操作是____________(填序号)。
A.滴定管用蒸馏水洗后未用标准碱液润洗,直接装入标准碱液
B.滴定前滴定管尖端有气泡,滴后气泡消失
C.滴定管读数时,滴定前仰视滴定后俯视
D.待测液中指示剂酚酞(为有机弱酸)加得太多
(6)如果准确移取25.00mL 0.20mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?________ (填 “是”或“否”)用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列实验操作会引起测量结果偏高的是 [ ]
① 用天平称量NaOH固体,将小烧杯放在右盘,砝码放在左盘,并移动游码,使之平衡;
② 在配制烧碱溶液时,将称量后的NaOH固体溶于水,立即移入容量瓶,将洗涤烧杯的液体注入容量瓶后,加蒸馏水至刻度线;
③中和滴定时,锥形瓶内有少量水;
④酸式滴定管用蒸馏水洗后,未用标准液润洗;
⑤读取滴定管终点读数时,仰视刻度线。
A.① ② ③
B.② ④ ⑤
C.③ ④ ⑤
D.① ② ③ ④ ⑤下图是向100 mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图。根据图所得结论正确的是 
[ ] A.原来盐酸的物质的量浓度为1 mol·L-1
B.x处为含NaOH0.1mol的溶液
C.原来盐酸的物质的量浓度为0.1 mol·L-1
D.x处为含NaOH0.001mol的溶液用酚酞作指示剂,以0.100 mol·L-1的NaOH溶液测定装在锥形瓶中的一定体积的盐酸溶液的物质的量浓度。下列操作将导致测定值高于实际值的是 [ ] A.标准液在0刻度线以上,未予调整就开始滴定
B.碱式滴定管用蒸馏水洗涤后未用标准NaOH溶液润洗
C.观察记录滴定管内液面刻度时滴定前仰视,滴定后俯视
D.酚酞指示剂由无色变为红色时立即停止滴定某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100 mL稀H2SO4溶液;以0.14
mol/L的NaOH溶液滴定上述稀H2SO425.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14 mol/L NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00 mL,注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。
C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度0以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度0或0刻度以下。
E.检查滴定管是否漏水。
F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
a.滴定操作的正确顺序是(用序号填写):_________________ 。
b.该滴定操作中应选用的指示剂是:_____________。
c.在G操作中如何确定终点? ____________________。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”) ______________,原因是_______________________ 。
(3)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果精确到小数点后二位) ____________
mol/L。实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验。
请完成下列填空:
①配制100mL 0.10mol/L NaOH标准溶液。
②取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3 次,记录数据如下。
(1)碱式滴定管用蒸馏水洗净后在装碱液之前,还应该进行的操作是:_______________________。
(2)滴定达到终点的现象是______________________。
(3)根据上述数据,可计算出该盐酸的浓度约为______________。(保留两位有效数字)
(4)除去碱式滴定管中气泡的方法应采用操作______________________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。(填序号)
(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有__________。(多选扣分)
A.滴定前平视读书,终点读数时仰视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后又用标准盐酸润洗
D.称量前NaOH固体中混有Na2CO3固体
E.配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F.碱式滴定管尖嘴部分有气泡,滴定后消失某学生欲用已知物质的量浓度的HCl测定未知浓度的NaOH溶液,将HCl置于滴定管,氢氧化钠溶液置于锥形瓶,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定未知浓度的NaOH溶液,滴定到终点时锥形瓶中颜色变化为______________。
(2)下列操作中可能无法会怎样影响所测NaOH溶液浓度(填偏大、偏小或不影响)
A.酸式滴定管未用标准浓度的HCl润洗就直接注入标准盐酸___________
B.读数时,开始平视,结束时俯视液面___________
(3)某学生根据3次实验记录有关数据如下
请选择合理的数据计算NaOH溶液的物质的量浓度:c(NaOH)=________________。 某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至0刻度线以上
② 固定好滴定管并使滴定管尖嘴充满液体
③ 调节液面至0或0刻度线稍下,并记下读数
④ 移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤ 用标准液滴定至终点,记下滴定管液面读数。
请回答:
(1)以上步骤有错误的是(填编号)_________,该错误操作会导致测定结果___________(填“偏大”、“偏小”或“无影响”)
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,测定结果_______________(填“偏大”、“偏小”或“无影响”)
(3)判断滴定终点的现象是:______________________
(4)下图是某次滴定时的滴定管中的液面,其读数为__________mL
下面是一段关于酸碱中和实验操作的叙述:
①取一锥形瓶,用待测NaOH溶液润洗两次。
②在一锥形瓶中加入25 mL待测NaOH溶液。
③加入几滴石蕊试剂做指示剂。
④取一支酸式滴定管,洗涤干净。
⑤直接往酸式滴定管中注入标准酸溶液,进行滴定。
⑥左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶。
⑦两眼注视着滴定管内盐酸溶液液面下降,直至滴定终点。
文中所述操作有错误的序号为[ ] A.④⑥⑦
B.①⑤⑥⑦
C.③⑤⑦
D.①③⑤⑦用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答
(1)准确称取4.1g烧碱样品,所用主要仪器是____________________________。
(2)将样品配成250mL待测液,需要的仪器有_________________________________。
(3)取10mL待测液,用______________________量取。
(4)用0.2010 mol·L-1标准盐酸滴定待测烧碱溶液,滴定时________手旋转_________式滴定管的玻璃活塞,____________手不停地摇动锥形瓶,两眼注视________________,直到滴定终点。
(5)根据下表数据,计算待测烧碱溶液的浓度:_____________________。
(6)根据上述各数据,计算烧碱的纯度:__________________________。 某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室标准NaOH溶液对其进行滴定以测定它的准确浓度,完全反应时所得溶液pH大致为9。下表是4种常见指示剂的变色范围 
(1)该实验应选用__________作指示剂。
(2)下图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为________mL;反应达滴定终点时的现象为_________________________。
(3)为减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下 
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是_________。
A.实验结束时,俯视刻度线读取滴定终点时NaOH溶液的体积;
B.滴定前滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液;
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗;
D.锥形瓶预先用食用白醋润洗过;
E.滴加NaOH溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定。
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):C=_________mol/L。某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步: ① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②使滴定管尖嘴充满液体, 固定好滴定管
③ 调节液面至“0”或“0”刻度线稍下,并记下读数
④ 移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤ 用标准液滴定至终点,记下滴定管液面读数。
请回答:(1)以上步骤有错误的是(填编号)________,该错误操作会导致测定结果 (填“偏大”.“偏小”或“无影响”)__________________
(2)判断滴定终点的现象是:锥形瓶中溶液从 _______ 色变为_____________色,且半分钟不变色。(3)下图是某次滴定时的滴定管中的液面,其读数为 _________ mL
(4)根据下列数据:请计算待测盐酸溶液的浓度:___________________ 
常温下,浓度均为0.1 mol·L-1的四种溶液:①Na2CO3溶液 ②NaHCO3溶液 ③盐酸 ④氨水
试回答下列问题:
(1)上述溶液中有水解反应发生的是__________(填编号,下同), 溶液中溶质存在电离平衡的是
____________________;
(2)比较①、②溶液,PH值较大的是____________________;
(3)在溶液④中加入少量NH4Cl固体,此时 的值将_________(填“变小”,“变大”或“不变”);
的值将_________(填“变小”,“变大”或“不变”);
(4)用溶液③滴定V mL溶液④,其滴定曲线如图所示
①试分析在滴定过程中,滴定曲线上a、b、c、d四点: 水的电离程度最大的是___________点;
②取少量c点溶液于试管,再滴加0.1 mol/L NaOH溶液至中性。此时溶液中除H+、OH-外,其它离子浓度由大到小的顺序是________________________。
- -0.2的倒数是 .
- 日本将一些工业移往东南亚的原因是A.帮助东南亚国家发展经济B.日本国内缺乏科技人员 C.日本资金短缺D.靠近东南亚的原料
- 如图所示的四个家系,黑色是遗传病患者,白色为正常或携带者,下列有关叙述正确的是 [ ]A.可能是白化病遗传的家系
- 下列各句没有语病、内容明确的一项是[ ]A. 国家自从明确了全国统一的“五一”“十一”放假日之后,中国的假日经济
- 市区内各路口处画有停车线,当信号灯黄灯开启时司机应开始刹车,红灯开启时车不能越过停车线,否则违反交通规则.设黄灯开启经3
- 函数f(x)=-x3+2ax2+1(a∈R)在区间(0,23)上递增,[23,+∞)上递减,则实数a的值为 _____
- —Why? Where is the key to the meeting room? —Dear me! You __
- 关节活动起来非常灵活,与之有关的结构特点是关节结构里有( )A.关节软骨和韧带B.关节头和关节窝C.关节软骨和滑液D.
- 如图1,B是长度为1的线段AE上任意一点,在AE的同一侧分别作正方形ABCD和长方形BEFG,且EF=2BE.(1)点B
- 我国实行计划生育的目的是 [ ] ①控制人口数量 ②晚婚晚育 ③提高人口素质 ④少生优生A.①③B.②③ C.
- 角α的终边上有一点P(m,5),且cosα=m13,(m≠0),则sinα=( )A.513B.-513C.1213或
- 下列因式计算得代数式xy2﹣9x的是[ ]A.x(y﹣3)2B.x(y+3)2C.x(y+3)(y﹣3)D.x(
- 下列各式一定为正数的是[ ]A.(a+b)2B.2004|a|C.a2+b2D.2x2+3x4+
- 无产阶级第一次武装夺取政权和建立无产阶级专政的伟大尝试是[ ]A.成立巴黎公社B.成立共和国C.组织临时政府D.
- 近代有一位思想家主张学习西方,在其著作中提出了“物竞天择,适者生存”的观点。这位思想家是[ ]A.詹天佑B.严复
- 如图5-36所示四个钢铁工业城市,其区位类型与其他三个不同的是( )图5-36
- 佛教、道教是两种不同的宗教文化,而在我国的南岳衡山,南岳大庙两侧各有八座道观、佛寺,开门相见,香火相通,道士、僧人轮流值
- 有关我国农业生产的叙述,错误的是( )A.我国农耕区的畜牧业,以畜禽饲养为主B.我国四大牧区指的是内蒙古、新疆、青海、
- 1942年1月26日,《联合国家宣言》发表,宣言由美英苏中四国领衔,其余22国按国名的英文依次排列,这表明( )①
- “鸟有反哺之情,羊有跪乳之恩”这句话给我们的启示是( )①我们要从小养成孝敬父母的习惯 ②父母养育了子女,理应得到子女
© 2017-2019 超级试练试题库,All Rights Reserved.